Nemogućnost začeća je problem s kojim se suočava sve više parova. S obzirom na povečanu učestalost medicinski pomognute oplodnje (MPO) kao izbora liječenja parova s problemom začeća, konstantno je potrebno usavršavati metode koje se upotrebljavaju u IVF laboratoriju kako bi osigurali što veću vjerojatnost za rođenje jednog zdravog djeteta.
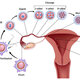
Razvoj zametaka počinje u jajovodu, spajanjem sjemene i jajne stanice (oplodnja) nakon čega nastaje zigota. Iz zigote diobama nastaje zametak (cleavage stage embryo) koji svakom diobom povećava broj stanica (blastomera) i nastavlja put kroz jajovod prema maternici.
Preimplantacijski razvoj zametka
Zametak u maternicu dolazi u stadiju morule i sposoban je implantirati se u endometrij maternice tek u stadiju blastociste, kada je u mogućnosti komunicirati s endometrijem receptorima koji se nalaze na površini trofoblasta.
Zametak u stadij razvoja koji zovemo blastocista dolazi 5. ili 6. dan nakon oplodnje i taj stadij se in vivo događa u maternici. Blastocista se sastoji od embrionalnog čvorića (ICM-Inner Cell Mass) od kojeg daljnjim diobama nastaje plod, blastocela odnosno središnje šupljine koja je ispunjena tekućinom i trofoblasta iz kojeg diobama nastaje posteljica.

Građa blastociste
Vrlo aktivna tema u znanstvenim krugovima je opravdanost transfera zametaka u stadiju blastociste. Vode se rasprave o prednostima i manama transfera zametaka 5. ili 6. dan u odnosu na transfer zametaka u stadiju diobe (cleavage stage embryo) 2. ili 3. dan.
Prednosti transfera blastociste
Razvoj medija za kultivaciju i poboljšanje uvjeta kultivacije omogućilo je produljenje in vitro kultivacije ljudskih zametaka bez bojazni da će im dulja izloženost in vitro uvjetima previše naštetiti.
U slučaju produljene kultivacije i transfera blastocisti postoji nekoliko prednosti;
- veća je mogućnost selekcije vijabilnih zametaka s manje kromosomskih abnormalnosti (zametci koji nemaju predispoziciju za razvoj i implantaciju te oni koji posjeduju greške u DNA ili u kromosomskoj građi, zaustaviti će razvoj u ranijim stadijima razvoja i neće doći do stadija blastociste)
- usklađivanje razvojnog stadija zametaka sa stanjem endometrija (zametci su sposobni implantirati samo u endometrij maternice oko 7. dana nakon ovulacije i samo u stadiju blastociste)
- smanjuje se opseg zamrzavanja, a zamrzavaju se potvrđeno vijabilni zametci s manje genetičkih nepravilnosti
- transferiramo najperspektivniji zametak čime se smanjuje postotak višeplodnih trudnoća (posebno značajno nakon uvođenja time-lapse tehnika za praćenje razvoja zametaka)
- transferi odmrznutih blastocista predstavljaju kategoriju transfera s najvišom uspješnosti ( u svježem ciklusu su zamrznute samo blastociste odlične kategorije koje se u postupku odmrzavanja vraćaju u endometrij koji nije pod utjecajem hormona stimulacije ovulacije)
- u slučaju preimplantacijske dijagnostike (PGS, PGD) kultivacija do stadija blastociste se favorizira zbog tehnika dobivanja stanica za analizu i mogućnosti odabira matičnih stanica na nešto većem stupnju diferencijacije (stanice embrionalnog čvorića i stanice trofoblasta)
- mogućnost opsežnijih, neinvazivnih metaboličkih istraživanja medija kulture blastocista kojima se nastoji saznati više informacija o vijabilnosti i sposobnosti zametaka
Nedostatak transfera blastociste
Ukoliko se sve oplođene jajne stanice iz svakog ciklusa drže u kulturi do 5. odnosno 6. dana, tada postoji rizik da u nekim ciklusima ni jedan zametak ne bude sposoban doći do stadija blastociste te u tim ciklusima neće biti vijabilnih zametaka koji bi se mogli vratiti u maternicu pacijentice.
Iako je dizajn medija za kultivaciju humanih zametaka napredovao i uvjeti kultivacije su izuzetno poboljšani, oni i dalje samo oponašaju uvjete u jajovodu odnosno maternici. Stoga se pretpostavlja da bi neki zametci, koji nisu pokazali sposobnost razvoja in vitro, in vivo uspjeli doći do stadija blastocite i implantirati se ukoliko se transfer učini raniji dan kultivacije.
Također, statističke analize su potvrdile da se transferom blastocisti povećava postotak monozigotnih blizanaca te da je povećan omjer spola u korist muške djece.
Kada se preporuča transfer blastocista
Produžena kultivacija zametaka i transferi blastocista pokazuju statistički pozitivne rezultate u postocima kliničkih trudnoća iz svježih postupaka, kumulativnim kliničkim trudnoćama (svježi zajedno sa odmrznutim postupcima) i postotku živorođene djece samo u slučaju kada se takva kultivacija provodi kod mlađih pacijentica koje nakon hormonske stimulacije jajnika produciraju više jajnih stanica (zadovoljavajući AMH) te na 3. dan kultivacije imaju 3 ili više odličnih zametaka.
Ukoliko produljenu kultivaciju prakticiramo kod pacijentica s lošijim prognozama; s nižim ovarijskim rezervama, niskim AMH, starije od 38 godina, s prisutnošću endometrioze, uzastopnim neuspjelim pokušajima MPO, u tom slučaju transferi blastocista neće rezultirati povećanim kliničkim trudnoćama ili postocima živorođene djece te se kod takvih pacijentica preporuča transfer zametaka u ranijim stadijima kulture (cleavage stage embryo).
Možemo zaključiti da je pri odabiru načina kultivacije i dana transfera bitan individualizirani pristup temeljen na znanju i iskustvu. Ne smijemo zaboraviti da uspješni rezultati svakog postupka ovise o adekvatnoj hormonskoj stimulaciji kojom bi se trebale producirati kvalitetne jajne stanice, uspješno izvedena oplodnja i optimizirani uvjeti kultivacije zametaka do stadija blastociste te priprema endometrija i atraumatski transfer zametaka.